(2) アンモニア水を加えると沈殿が生じ,過剰に加えると溶ける。 1 2 (8) 鉛(ii)イオンを含む水溶液に,(1)希塩酸,(2)クロム酸カリウム水溶液を加えたときに生じる沈殿の化学式と色をそれぞれ記せ。 1 2 電離式の一覧です。中学生の勉強に使えます。電離式、イオン式、化学式の違いや、練習問題もあります 酸性の水溶液になる電離式 ③ アンモニアが水に溶けたときの電離化学名又は一般名 アンモニア水 (Aqua ammonia) (aqeuous ammonia) 別名 水酸化アンモニム (Ammonium hydroxide) 濃度又は濃度範囲 100% 分子式 (分子量) NH4OH (351) 化学特性 (示性式又は構造式) CAS番号 官報公示整理番号(化審法) (1)314 官報公示整理番号(安衛

高校化学 アンモニアの製法 練習編 映像授業のtry It トライイット
アンモニア水溶液 化学式
アンモニア水溶液 化学式-アンモニウム (ammonium)は、化学式NH 4 の分子イオンである 。 アンモニア (NH 3)のプロトン化によって形成される。13 名称Ammonium nitrate種別一般用試薬 (研究実験用)化学式NH4NO3危険等級Ⅰ労働安全衛生法の表示労57,572危険物の類別第一類危険物の品名硝酸塩類危険物の数量500mL特性可燃性・引火性ガス、健康有害性平均分子量8004危険物の性状第1種CAS登録番号 14 名称1mol/L (1N) 硝酸等級なし規格規定液 VS濃度




頻出 化学反応式 16 化学がちょっとだけ好きな社労士
アンモニア水溶液が塩基性を示す理由は、解けたアンモニアの一部が水分子と反応し、その際、水分子がもとになって oh が発生するからである。 つまり、アンモニアの場合、 または塩基1化学式が受け取ることができるh イオンの数ともいえる。例とし硝酸銀水溶液 アンモニア水 硝酸銀アンモニア溶液とは コトバン デジタル大辞泉 硝酸銀アンモニア溶液の用語解説 硝酸銀の水溶液にアンモニア水を加えて酸化銀を沈殿させ、さらにその沈殿が消えるまでアンモニア水を加えたもの。Start studying 水溶液の電離式、化学反応式 Learn vocabulary, terms, and more with flashcards, games, and other study tools
化学式とは元素記号を用いて物質を表したものである。 化学式には分子式や組成式がある。 分子構造をとらないイオン化合物などでは 分子式と言わずに組成式というべきである。 たとえばNaCl(食塩)は組成式で、CO2は分子式である。水溶液を加えて塩基性にした後,少量の硫酸銅(且)水溶液を加えると赤紫色を呈 した。ペプチドxの水溶液に濃硝酸を加えて加熱し,冷却後にアンモニア水を ② 加えて塩基性にすると橙黄色を呈した。ペプチドxの水溶液に塩化鉄(皿)水溶 液を加えると青紫色を問7 次の文章中の( )内に適当な化学式・文字式・数値を入れて文章を完成せよ。 0010mol/L酢酸ナトリウム水溶液の加水分解度h、加水分解定数Kh、pHを求める。酢酸ナトリウムは 電解質なので次のような電離反応式で各イオン種に電離する。
必ず、水溶液として使用する。 溶解度曲線図 > 3) 塩化アンモニウム (塩安) Ammonium chloride 化学式 NH 4 Cl = 53.49化学式 nh4oh 化学物質を特定できる一般的な番号 cas rn: 濃度又は濃度範囲 アンモニア水 100%(①アンモニア、②水) 可燃性(固体、気体) アンモニア水溶液は不燃性だが、アンモニアガスが放出することに気体のアンモニアnh 3 を過剰の硫酸h 2so 4 に完全に吸収させる。そして,未反応の h 2so 4 を ② 濃度のわかっている水酸化ナトリウムnaoh 水溶液で中和滴定する。このことから nh 3 の物質量を求めるという流れである。
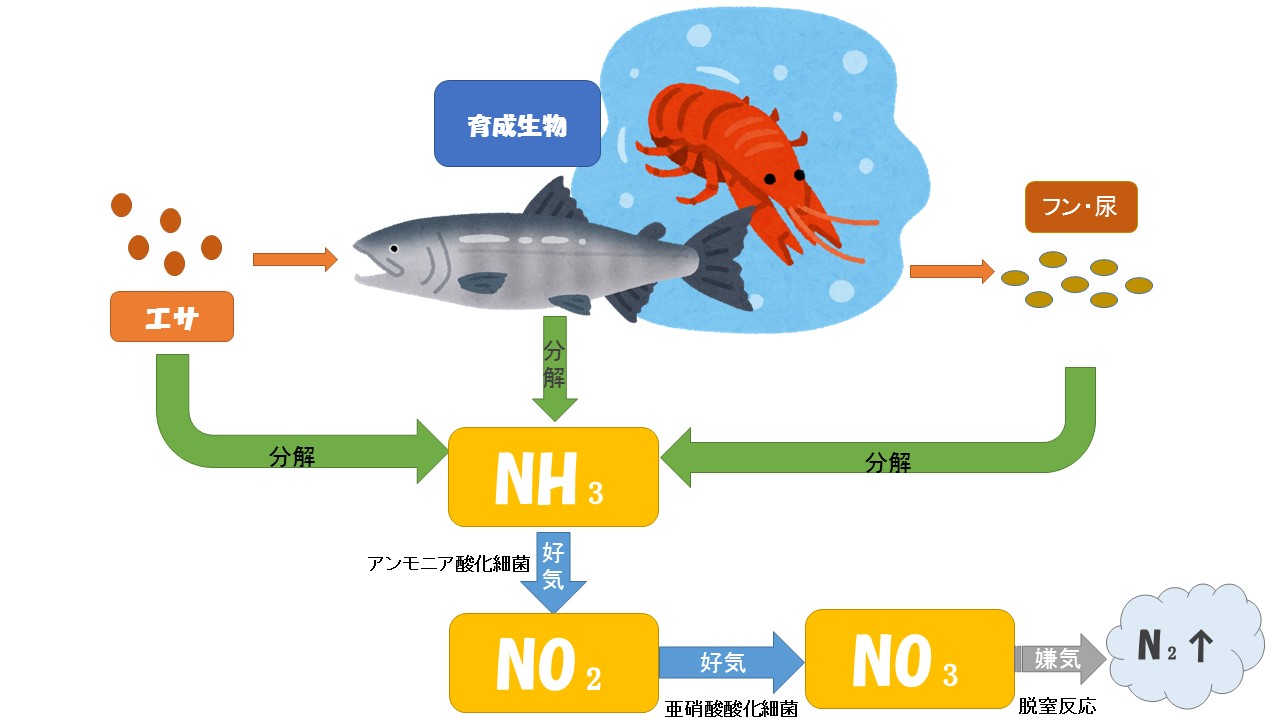



水質管理 窒素循環について アンモニア 亜硝酸 硝酸 持続可能な農業 養殖ビジネス



アンモニアはなぜアルカリ性を示すのか アンモニアの特徴とともにわかりやすく解説 ジグザグ科学 Com
ンモニア水溶液100 を水で希釈して010mol/ のアンモニア水溶液を得た。 問1 加えた水の量は何 か。有効数字2桁で答えよ。ただし,飽和アンモニア水溶液の密度は 00kg/ である。ただし,混合に伴う体積変化はないものとする。酢酸-酢酸ナトリウム緩衝液 CH COO CH COOH H Ka CH COOH H CH COO Ka CH COOH H O H O CH COO 3 3 3 3 3 2 3 3 − − − = × = ↔ CH COOH CH COO pH pKa log CH COOH CH COO log Ka 1 log Ka CH COOH CH COO log H 1 log 3 3 3 3 3 3 − − − = = × = HendersonHasselbalchの式 12 01 mol/L 酢酸と 02 mol/L 酢酸ナトリウム水溶液のpH CH NH3 (アンモニア)H2O (水)=NH4OH (アンモニア水) まず、これが違う。 アンモニア水は、アンモニアが水に溶けているだけで、水と化合しているわけじゃない。 なので、 とは書かない。 食塩水を化学式で以下のように表さないのと同じ。 で、アンモニアは、水に溶けると一部が電離して、アンモニウムイオンと水酸化物イオンを生じる。 化学式で表すと、以下の通り




化学工業の歴史1 無機 有機化学工業の基盤成立 化学工業の基礎知識2 ものづくり まちづくり Btob情報サイト Tech Note




高校化学 アンモニアの製法 練習編 映像授業のtry It トライイット
水酸化アンモニウム (ammonium hydroxide)は、 アンモニア の 水溶液 を示す場合に用いられる名称である。 アンモニア水 (ammonia water)とも呼ばれ、 NH3 (aq)と表すことができる。 アンモニア水中の電離平衡において中間体として NH4OH の存在が仮定されたこともあるが 、この 化学種 の存在は否定されている 。 化学式 で NH 4 OH− と塩のように表すが、この化学種の化学式 (NH 4) 2 S、式量681。 アンモニア水に硫化水素を飽和させてつくった硫化水素アンモニウムNH 4 HSの水溶液に当量のアンモニア水を混合し、零下18℃に冷却すると、針状結晶として析出する。混合水溶液を調製した。 (a)混合水溶液におけるアンモニアのモル濃度CIとアンモニウムイオンのモル 濃度aをそれぞれ答えなさい。ただし,堀ヒアンモニウムの溶解による溶 液の体積変化はないものとする。 (b)混合水溶液の水素イオン濃度町を答えなさい。



2 o 問1 次の各化学反応式に係数を入れよ




水素水アンモニアメタンの化学式と分子モデル化学学校ノートブック檻の中の紙のシート 3dのベクターアート素材や画像を多数ご用意 Istock
アンモニア(NH3)の電離式を教えてください! Clear ぱぴこがーる。 水酸化ナトリウム水溶液の電気分解の式では、 「電離式」はnaoh→na()oh() 「化学反応式」は2h(2)o→2ho(2)と教科書に書いてあります。 どちらも同じものな硝酸亜鉛(II)水溶液にアンモニア水を加えれば水酸化亜鉛を沈殿する。 水酸化亜鉛(II)は塩化アンモニウム水溶液に溶ける。 アンモニア水1滴 攪拌後 塩化アンモニウム溶液 10滴 問題 5 以下の反応について,化学反応式を書け。 水酸化亜鉛(II)は塩化アンモニウム水溶液に溶ける 解答




イオン式 電離式まとめ 中学理科 ポイントまとめと整理
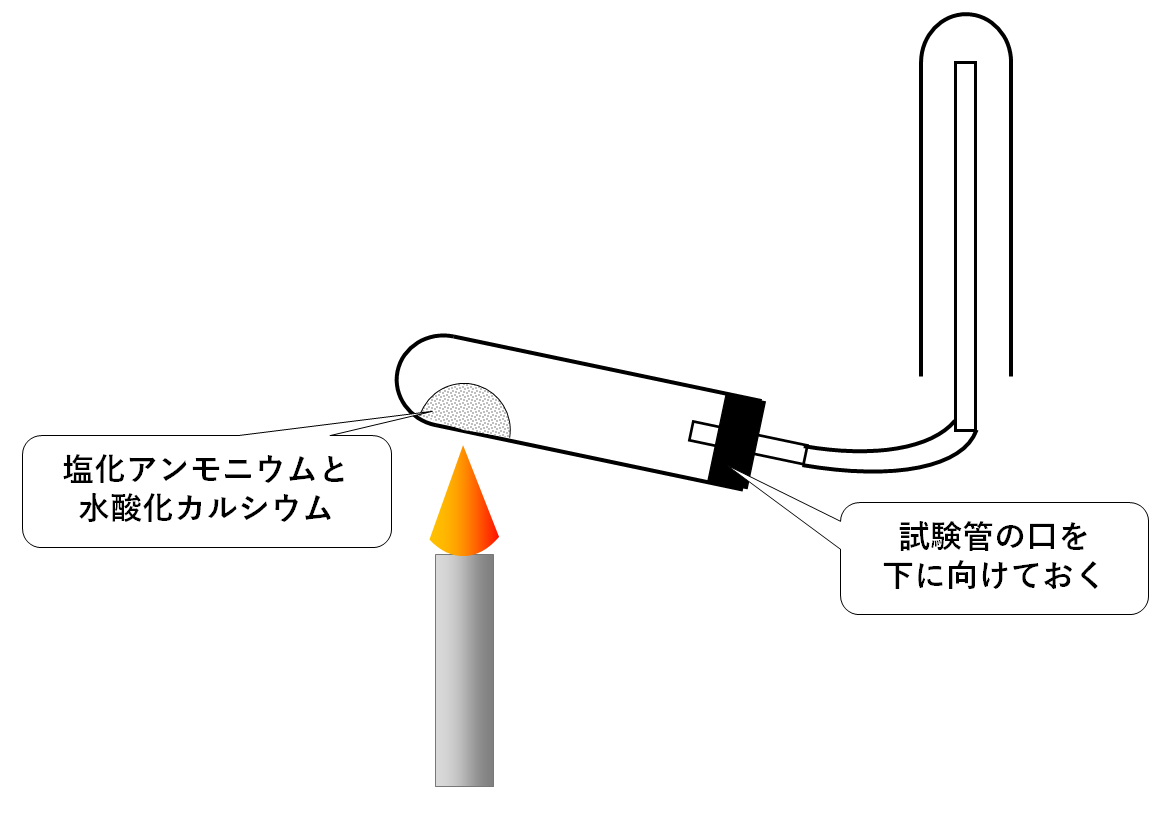



中3化学 アンモニアの利用 中学理科 ポイントまとめと整理
そこで、金属イオンを含む水溶液に、アンモニア nh 3 水や水酸化ナトリウム naoh 水溶液を少しずつ加えていくと、次の表2 のように変化します。 アンモニア水を加えていった場合でも、アンモニア NH 3 は弱塩基なので、生じた水酸化物イオン OH によって濃度未知の塩酸100ml を0100ml/l の水酸化ナトリウム水溶液で中和したら125ml を要した。この塩酸の濃度は何mol/l か。 (4) 酢酸の濃度を決めるため,水酸化ナトリウム水溶液で中和滴定した。このとき使用する指示薬は,次のどれが適当か。化学名 アンモニア水(水酸化アンモニウム) 化学式 NH 4 OH 英語名 ammonia solution, ammonia water, ammonium hydroxide アンモニア水の特徴 アンモニアガスの水溶液で、薬局で市販されているものは10%溶液です。比較的手軽に入手できます。 やや強いアルカリ性を示します。




6 1 酸と塩基 おのれー Note




頻出 化学反応式 16 化学がちょっとだけ好きな社労士
また、アンモニア性硝酸銀水溶液の作り方は次の通り。 硝酸銀水溶液にアンモニア水を加えると、褐色の酸化銀Ag 2 Oの沈殿を生じる。 2 A g 2 O H − → A g 2 O H 2 O アンモニアを水に溶かすと、以下の式のようになります。 NH3 H2O→NH4 OH そのため、アルカリ性になります。 6人 がナイス!16.窒素と水素を化合させると,アンモニアが生成する。 N2 +3H2 →2NH3 17.硝酸銀水溶液に塩化ナトリウムを加えると,白い沈殿を生じる。 AgNO3 +NaCl →NaNO3 +AgCl
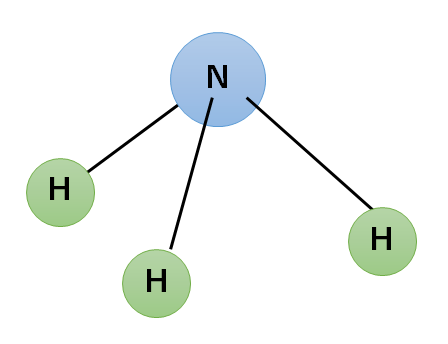



中3化学 アンモニアの利用 中学理科 ポイントまとめと整理



3
化学名又は一般名 アンモニア 別名 無水アンモニア、(Ammonia anhydrous)、アンモニアガス、(Ammonia gas) 濃度又は濃度範囲 100% 分子式 (分子量) NH3 (1703) 化学特性 (示性式又は構造式) CAS番号 官報公示整理番号(化審法) (1)391 官報公示整理番号・薄い水溶液は苦味があり、手につくとぬるぬるする 酸の濃塩酸と、塩基の濃アンモニア水を用意します。 上の化学反応式 よ,2 CoH Ca 0, × 0x 10 2 210 X (03 250 mL に水を加えて1Lとするを,濃度は本 になるので or x (0 = °3 015× (0 ち0 ×10 ニ ke 70x104 1c0x10 = 2,0 X (0 Cor 50×104 よって H= 1ago H" 10g10 ( × (05") 030 11 107 ニ (1



Http Nikken Net Contents 401 04 1 Siryo 0101 Pdf




1 B 2 C 1 1 9 Descubre Como Resolverlo En Qanda
アンモニアは常温で気体状態です。 アルカリ性とは水溶液の性質 ですので、アンモニアが水に溶解してできたアンモニア水がアルカリ性を示すということです。 アンモニアが水に溶けるときは、以下のように反応します。 NH 3 H 2 O ⇄ NH 4 OH – アンモニア自体はNaOHやKOHのように電離しませんが、水と反応することでアンモニウムイオンNH 4 とOH – を生成しアンモニアソーダ法(ソルベー法)の反応式を1つにまとめる 赤鉄鉱(酸化鉄 (Ⅲ)を含む)と,十分量の一酸化炭素を反応させる 酸化アルミニウムを水酸化ナトリウム水溶液に加える 水酸化アルミニウムを強熱する ケイ酸ナトリウムに塩酸を加える 1 (ア) ~ (カ) に適当な式 ((イ) はイオン反応式) を記せ。 2 25 ℃におけるアンモニアの電離定数は 160 × 105 mol/L である。塩化アンモニウムの加水分解定数 K h を求めよ。 水のイオン積 K w =100 × 1014(mol/L) 2 3 100 × 102 mol/L の塩化アンモニウム水溶液の pH を
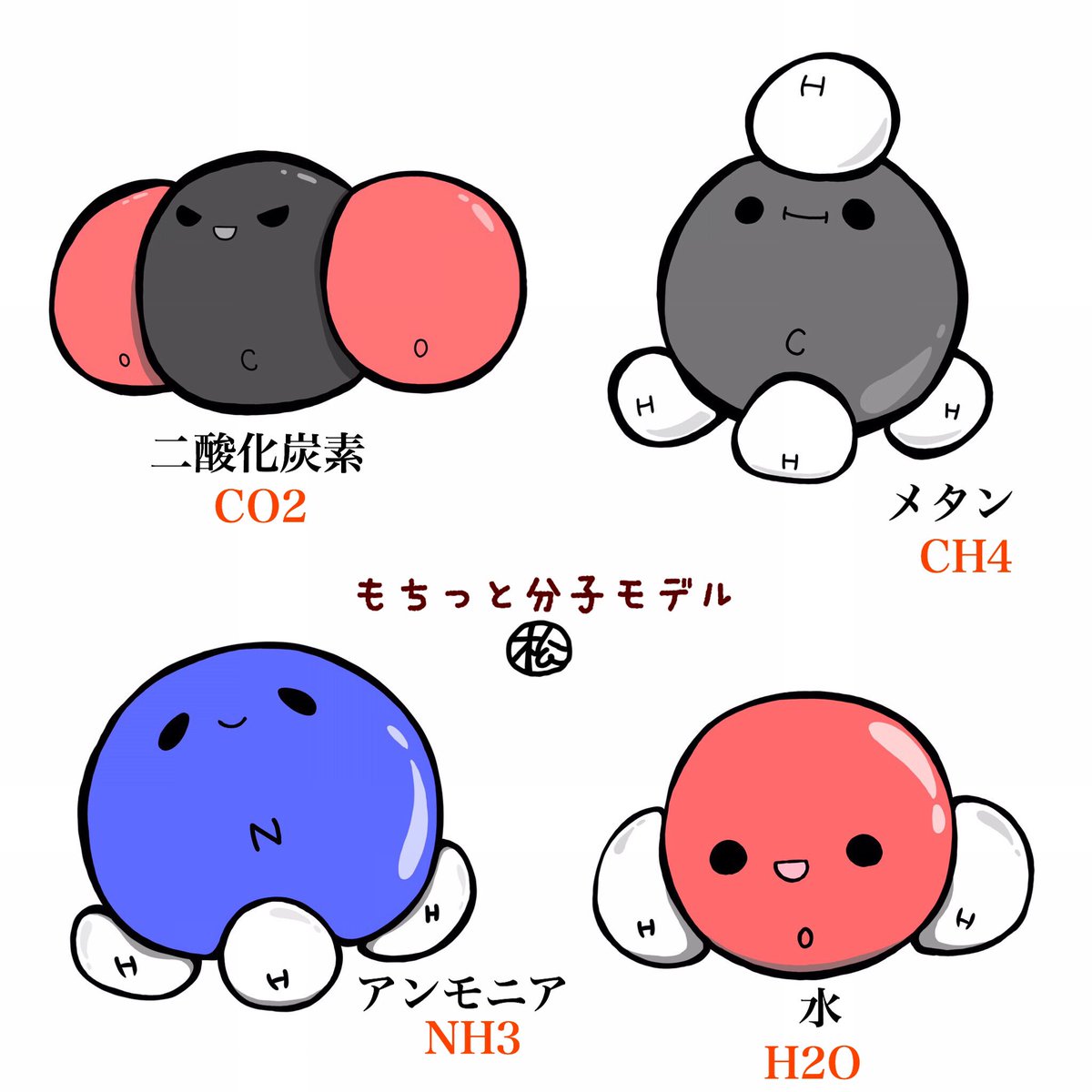



化学式




アンモニア水とテトラアンミン亜鉛 の化学式についてですが なぜアンモニアは4mo Clear
硝酸ビスマス水溶液に過剰量のアンモニア水を加えると,白色の水酸化ビスマスを生ずる。 解答 Bi 3+ +NO 3 - +2NH 3 +2H 2 O → Bi(OH) 2 NO 3 ↓+2NH 4 + アンモニアの性質を中学生向けに詳しく解説! テストに出題されるアンモニアの性質は、このページを読めば完璧 だよ! 急いでいる人のために、まずはアンモニアの性質のまとめを書いておくね。 アンモニア(化学式NH 3)の性質まとめ アンモニア水溶液は1価の弱塩基で、下式のとおり電離定数に従い電離平衡の状態にあります。 NH3+H2O⇔NH4 ()+OH () ・・・ (式1) 塩酸は1価の強酸で、下式のとおり完全電離していると考えて構いません。
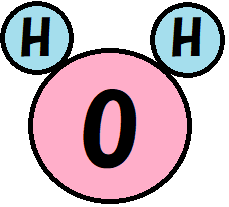



単体 化合物 純粋な物質 混合物の違いが読むだけでわかる



塩酸とアンモニアが完全に中和するときの化学反応式を書けという問題についてな Yahoo 知恵袋
ヨウ化カリウム 水溶液 硫酸銅(Ⅱ) 水溶液 過酸化水素水 ビタミンC入り ジュース 過マンガン酸カリウム 水溶液 + 硫酸 (+K3Fe(CN)6 aq) ① ② ( ) ③ ④ 過酸化 6 シュウ酸と過マンガン酸カリウムとの反応は何ですか?2 観測した反応に対する正味の




氷やアンモニア水は単体 純物質 化合物 混合物




頻出 化学反応式 16 化学がちょっとだけ好きな社労士
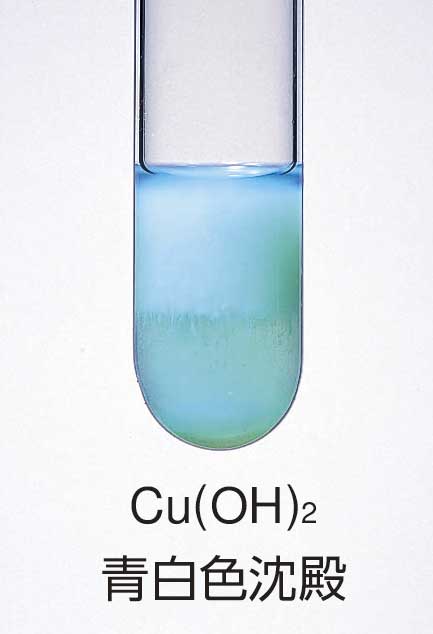



アクセス化学 例題解説 基本例題90 銅イオンの反応



酸と塩基 電離平衡




水溶液の性質まとめ 中学理科 ポイントまとめと整理




高校化学 水酸化アルミニウムの性質 映像授業のtry It トライイット




アクセス化学 例題解説 基本例題90 銅イオンの反応
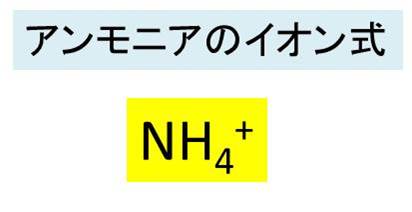



アンモニアの化学式 分子式 構造式 電子式 イオン式 分子量は イオン反応式は
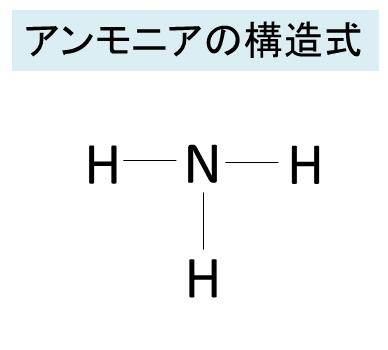



アンモニアの化学式 分子式 構造式 電子式 イオン式 分子量は イオン反応式は



Q Tbn And9gctchbfdn13afllusbqpkz Ohalrqtymd52ao Dhg Ndxtbpfrrs Usqp Cau




理科 中2 7 化学反応式の作り方 Youtube
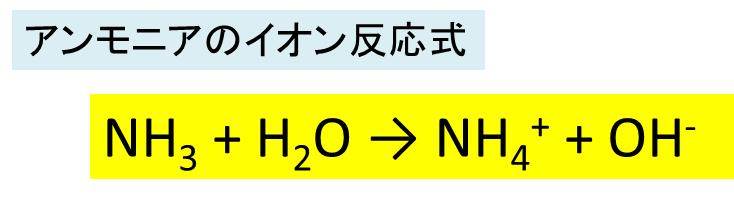



アンモニアの化学式 分子式 構造式 電子式 イオン式 分子量は イオン反応式は
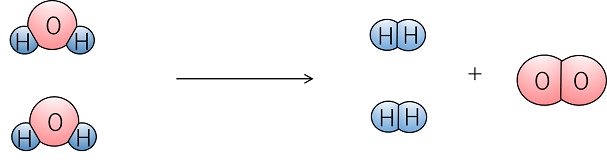



化学反応式




混合物と純物質




17 号 アンモニア合成装置 Astamuse
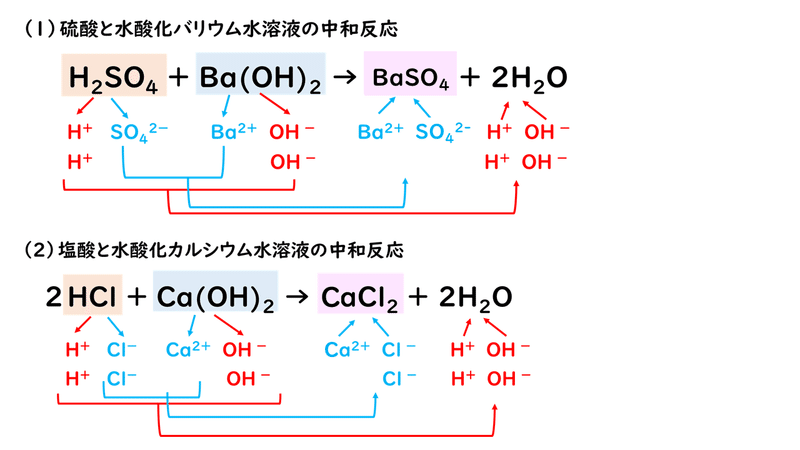



6 4 塩とその性質 おのれー Note



化学の質問です 酸化銀にアンモニア水を加える時のイオン反応式を答 Yahoo 知恵袋




実験8 9発熱反応 吸熱反応の導入について ラスカルのブログ




高校化学 水酸化亜鉛の反応 映像授業のtry It トライイット




高校化学 塩化アンモニウムの加水分解 映像授業のtry It トライイット




頻出 化学反応式 17 化学がちょっとだけ好きな社労士
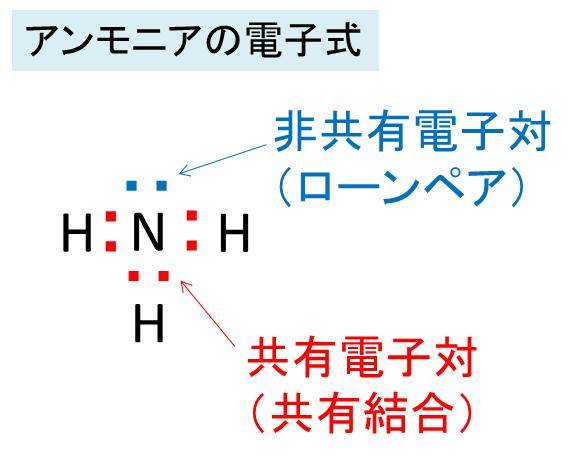



アンモニアの化学式 分子式 構造式 電子式 イオン式 分子量は イオン反応式は




高校化学基礎 塩基の価数 映像授業のtry It トライイット




頻出 化学反応式 4 化学がちょっとだけ好きな社労士



アンモニアと二酸化炭素の化学反応式の仕組みがわかりません 組み方 Yahoo 知恵袋




どうしてアンモニアの価数は3では無いのですか Clear



Http Www Keins City Kawasaki Jp 9 Ke9104 Jikken 30 Pdf




授業に潜入 おもしろ学問 自然科学科目群 化学 化学概論 I 中村敏浩 教授 京都大学広報誌 紅萠



下線部の反応はスルホ基を持つ化合物に濃アンモニア水を加えた反応です Yahoo 知恵袋




See How To Solve It At Qanda



アンモニア 水 硝酸の化学反応式を教えてください アンモニアと水で硝酸は Yahoo 知恵袋




完全版 入試に出るアンモニアの製法をまとめたった 化学受験テクニック塾




沖縄県名護市立名護中学校 理科 酸 アルカリと塩 化学変化とイオン 松田 晋介教諭



原子の手
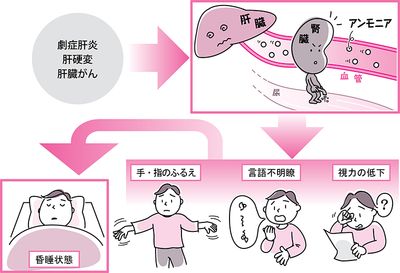



アンモニアとは コトバンク
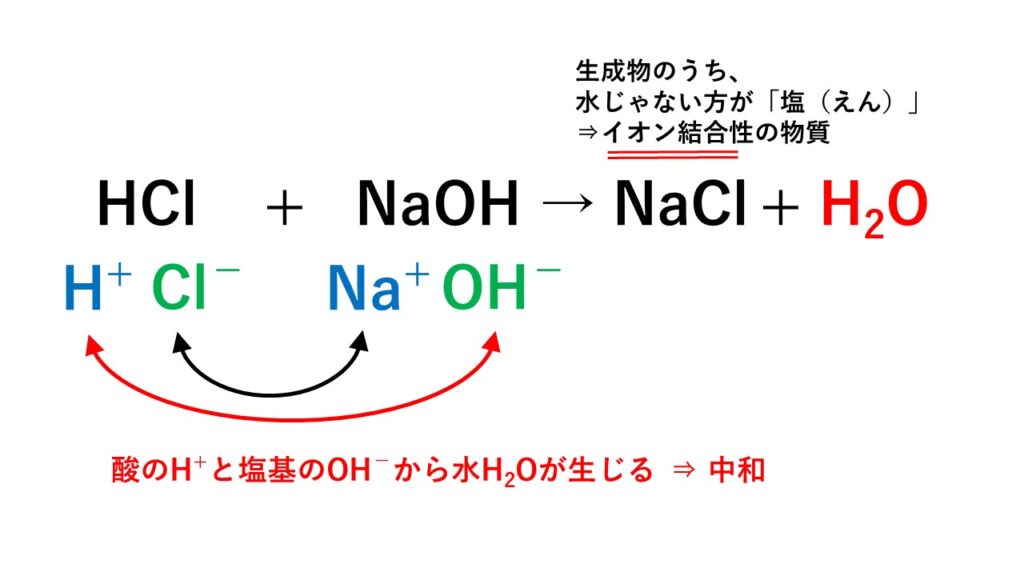



5分でわかる 中和反応とは 化学反応式と計算問題の解き方 練習問題付き サイエンスストック 高校化学をアニメーションで理解する




銀鏡反応の反応式の作り方と構造決定の使い方とまとめ 化学受験テクニック塾



気体に関する化学変化




アンモニア Nh3 の電離式を教えてください Clear



第57章 実験 鉄イオン
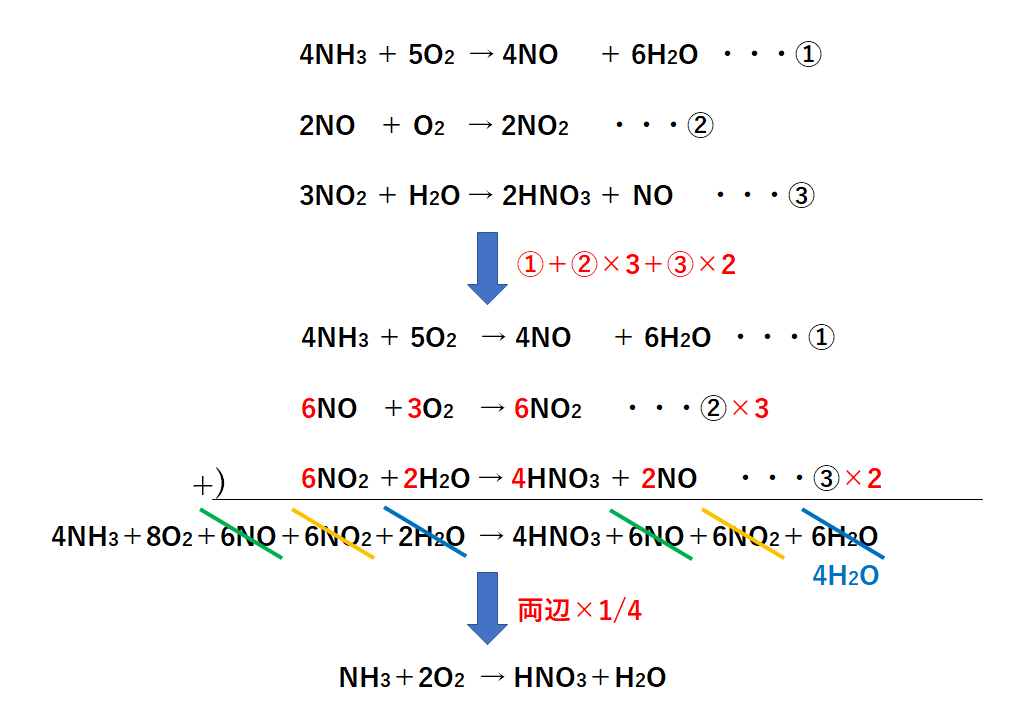



中3化学 アンモニアの利用 中学理科 ポイントまとめと整理




アクセス化学 例題解説 基本例題90 銅イオンの反応




1 Squar Lihat Cara Penyelesaian Di Qanda



実験13 アンモニアの噴水 1年理科 化学 Takaの授業記録12
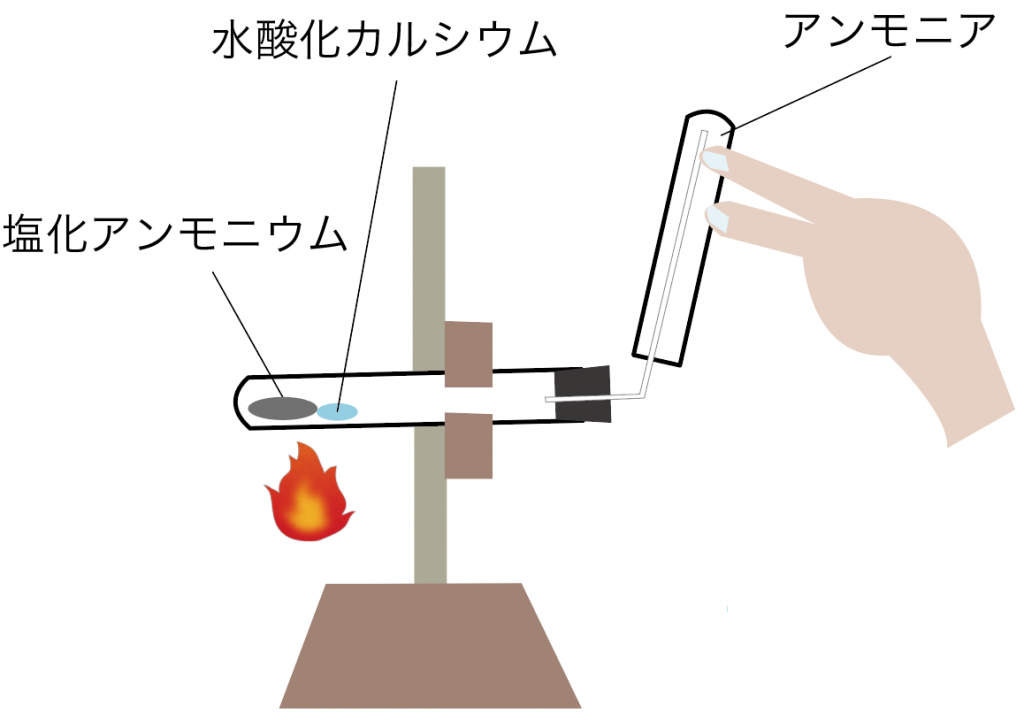



中1理科 3分でわかる アンモニアの発生方法 作り方 集め方 性質 Qikeru 学びを楽しくわかりやすく



2章a 類題1 4 0004 Top A 問題 次の各問いに答えなさい 問1 Cu2 と Fe3 を含む混合水溶液がある この2つの陽イオンを分離するために次の水溶液を使用した どちらが適切ですか 反応式を書いて説明しなさい 1 水酸化ナトリウム水溶液 2 アンモニア水




高校化学 水酸化亜鉛の反応 映像授業のtry It トライイット




質量パーセント濃度が28 の濃アンモニア水 0 90g Cm3 のモル濃度は何mol Clear
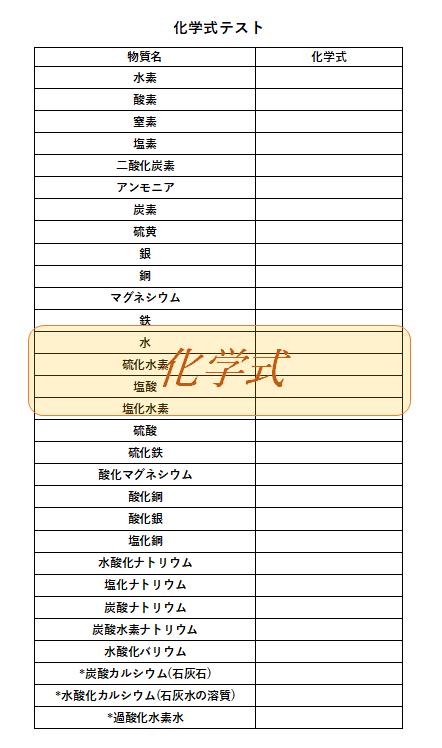



化学式記号 Tourotom1 1




質問です Clear
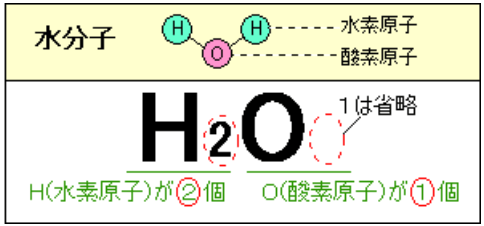



化学式の一覧や覚え方 中学生が覚えておきたい化学式 三重の個人契約家庭教師




銀が溶けた溶液に少量のアンモニア水を加えた時のイオン反応式をかけ 化学 教えて Goo
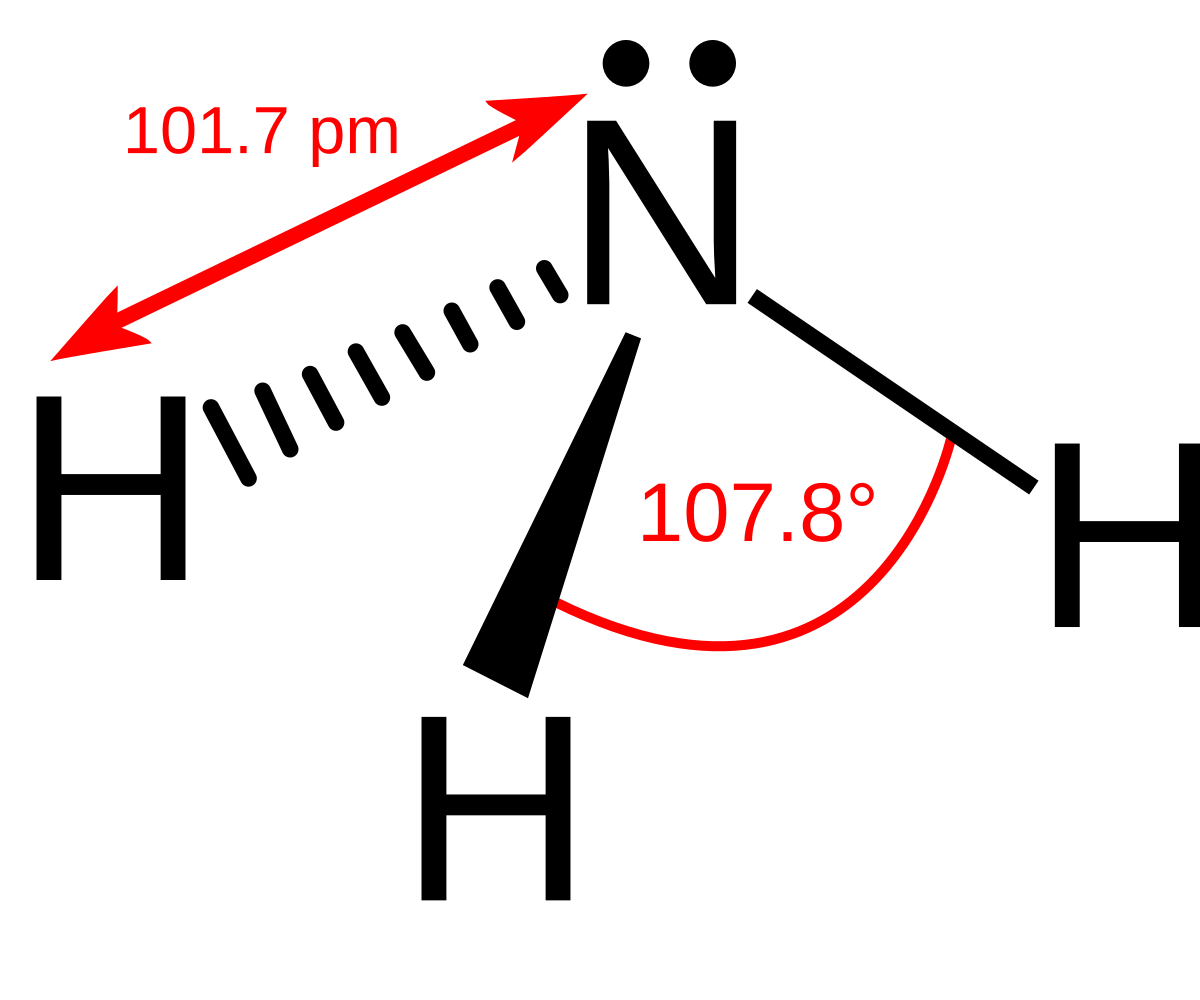



アンモニア Wikipedia



化学実験 Iv属 亜鉛



空気からパンを作る アンモニアの話 つくばサイエンスニュース



アンモニアと硫酸の中和の化学反応式の書き方か分かりません 途 Yahoo 知恵袋




アンモニア水の電離式を写真のように誤解しています どうして紫下線のような式になるか教 Clear




1 2 Lihat Cara Penyelesaian Di Qanda



5分でわかる 中和反応とは 化学反応式と計算問題の解き方 練習問題付き サイエンスストック 高校化学をアニメーションで理解する




汚れとお掃除の百科事典 ナチュラルクリーニング アンモニア水 サニクリーン
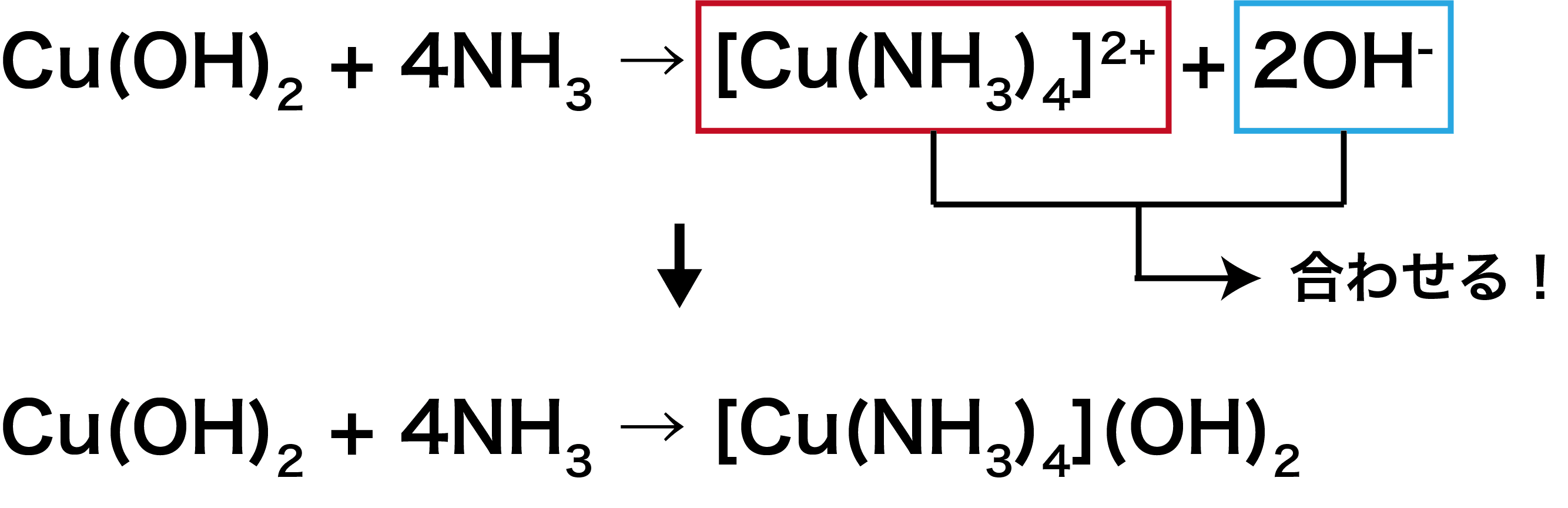



錯イオン 色 配位数 形 価数 命名法を総まとめ 化学のグルメ




なぜ中和で水を生じない場合があるのですか Clear




原子と分子 化学式 無料で使える中学学習プリント




アンモニアの性質まとめ 中学生用
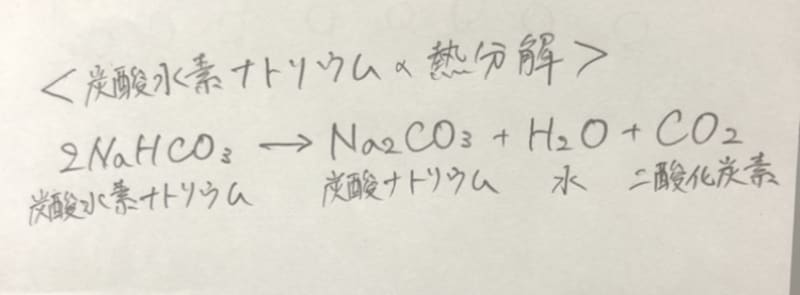



炭酸水素ナトリウムの化学反応式を教えてください アンサーズ



化学の質問です 2番と3番はどちらも大量のアンモニア水を塩化銀 酸化銀 Yahoo 知恵袋



炭酸アンモニウム Wikipedia
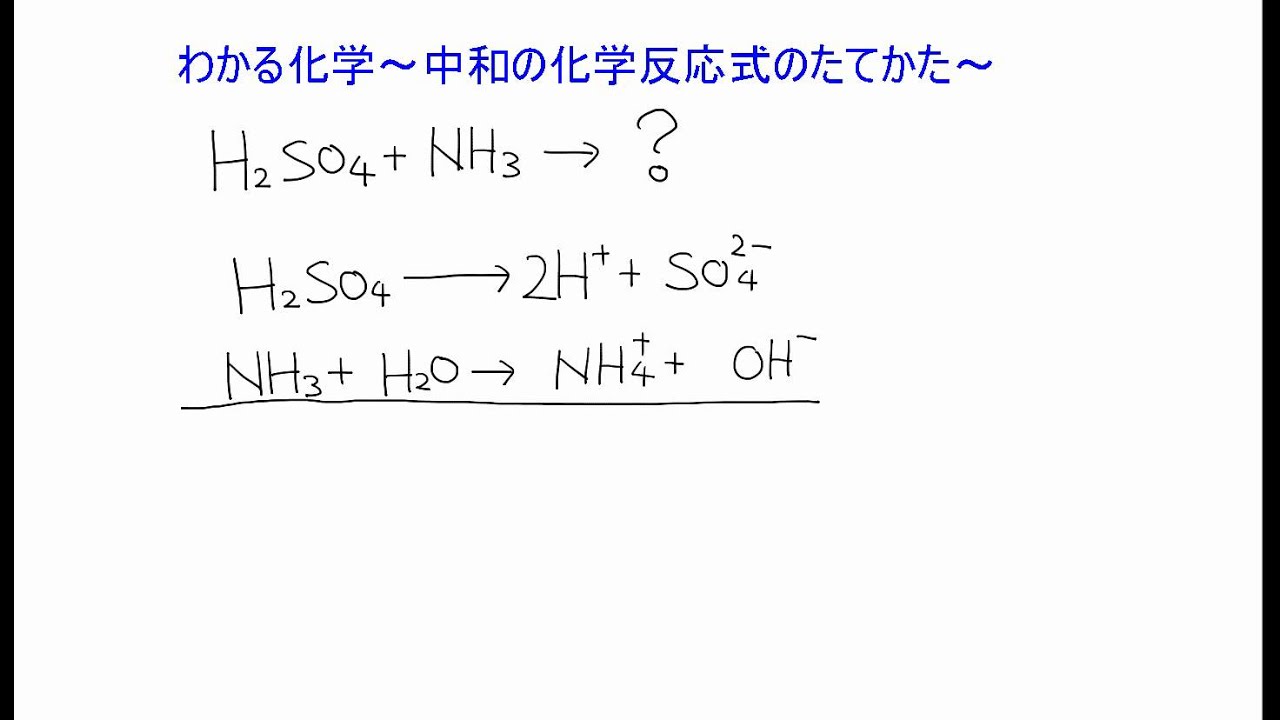



ゼミナールの化学基礎 中和の化学反応式のたてかた Youtube




010 Mol Y L 500 Ml Mol Lihat Cara Penyelesaian Di Qanda




基本例題 基本例題073 アンモニアソーダ法 ソルベー法 反応式 Youtube
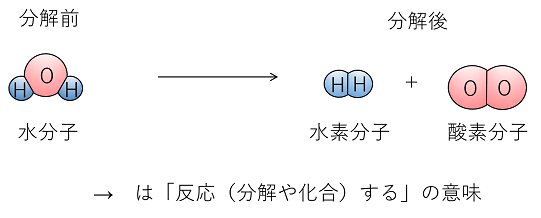



化学反応式




中1 理科 化学 アンモニアの発生 12分 Youtube



アンモニア You Iggy




尿素scrシステムについて アドブルーと同等品質の尿素水なら低価格のオプティ エコツーライト




1 Lihat Cara Penyelesaian Di Qanda




水素水アンモニア暗い青色の背景上でのメタンの化学式と分子モデル アイコンのベクターアート素材や画像を多数ご用意 Istock



第55章 実験 アルミニウムと亜鉛




3分でわかるアンモニアの発生方法 中学理科のすゝめ 定期考査対策から受験まで
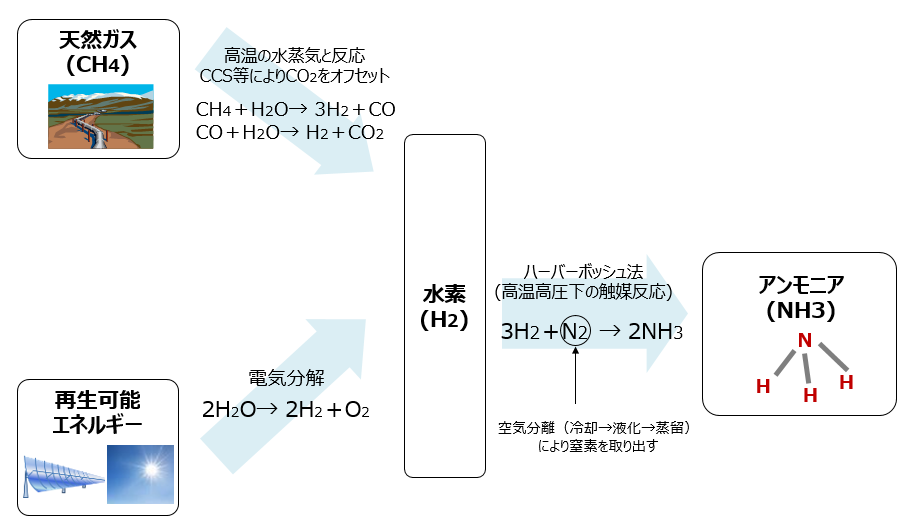



アンモニアが 燃料 になる 前編 身近だけど実は知らないアンモニアの利用先 スペシャルコンテンツ 資源エネルギー庁



Search Q E7 A1 Ab E5 8c 96 E6 B0 B4 E7 B4 A0 E9 9b E9 9b E5 8f Tbm Isch




水素 水 アンモニア メタンの化学式と分子モデル ベクトル図のイラスト素材 ベクタ Image



化学実験 Ii属 銅



実験 吸熱反応 2年理科 Takaの授業記録17



3




アンモニアと塩化水素の中和反応 化学がちょっとだけ好きな社労士




化学工業の歴史1 無機 有機化学工業の基盤成立 化学工業の基礎知識2 ものづくり まちづくり Btob情報サイト Tech Note


